Tratamento para a eliminação de iões dissolvidos na água através de resinas de troca iónica que são reativadas pela utilização de regenerantes.
O princípio da troca iónica consiste na troca de iões entre um sólido e um líquido, na qual não ocorre nenhuma alteração substancial na estrutura do sólido.
Como a troca de iões é uma reação reversível, o material de troca pode ser regenerado para novos processos.
Tipos principais:
Tecnologias
TROCA IÓNICA
- Desmineralização
- Catião – Anião
- Leito misto
- Desnitrificação
- Decarbonação
- Descalcificação
- Outros
APLICAÇÕES
- Como pós-tratamento de outros processos, por exemplo, osmose inversa
- Em processos industriais, associados a vários setores:
- Na indústria agro-alimentar
- Na indústria química e farmacêutica
- Nas indústrias da energia, eletrónica e nuclear
- Para tratamento de superfície
- Para abastecimento de água a caldeiras
- Para purificação da água (remoção de perclorato e urânio, entre outros)

FUNCIONAMENTO
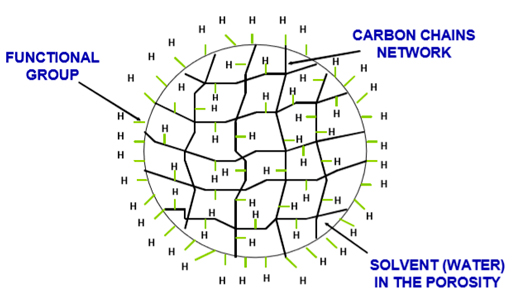
Os permutadores de iões são substâncias insolúveis em forma granular, tais como pequenas contas, chamadas resinas, que são capazes de absorver iões de uma solução e, em troca, renunciar a uma quantidade equivalente de outro ião sem qualquer alteração aparente na sua aparência física ou solubilidade. Esta troca só funciona entre iões de igual carga elétrica (catiões para catiões e ânions para ânions).
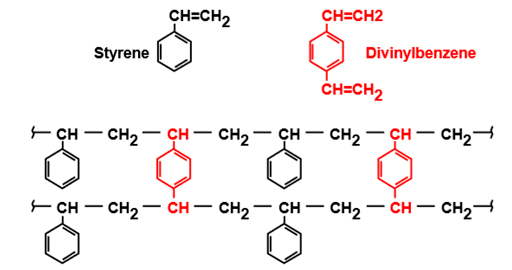
A resina mais comum é obtida por copolimerização do estireno e divenilbenzeno (DVB), que solidificam sob a forma de esferas em que o grupo de troca ativa é inserido.
Estas resinas terão uma superfície específica diferente e uniformidade em função do tipo de aplicação e do grupo ativo de radicais.
|
CATIÓNICA (C) |
STRONG (CF) Grupos sulfónicos (R-SO3) |
Regenerado com NaCl: Trocam catiões divalentes e trivalentes por iões de sódio. Trocam todos os tipos de cátions por H+. |
|
FUNCIONAMENTO (CD) Grupos carboxílicos (R-COOH) |
Regenerado com ácido forte: Trocam catiões ácidos e hidróxidos fracos por H+. | |
|
ANIÓNICA (A) |
STRONG (AF) Grupos de amónio quaternário |
Trocam ânions ácidos fortes e fracos (SiO2 , CO2, ácidos orgânicos) por grupos OH-. |
|
FRACAMENTE BÁSICO (AD) Grupos de amónio terciário |
Trocam aniões ácidos fortes (Cl-, SO4=, NO3) por grupos OH-. (Cl-, SO4=, NO3) por grupos OH- | |
| MODERADAMENTE BÁSICO | Misturado entre os dois anteriores | |
| ESPECIAIS | Macroporosa | Podem ser CF, CD, AF, AD e têm maior resistência mecânica, à temperatura e aos oxidantes. |
| Metal seletivo | São CF regenerados com ácido | |
| Scravanger ou adsorventes | São AF microporosas e retêm matéria orgânica e colóides. Regeneram-se com NaCl |
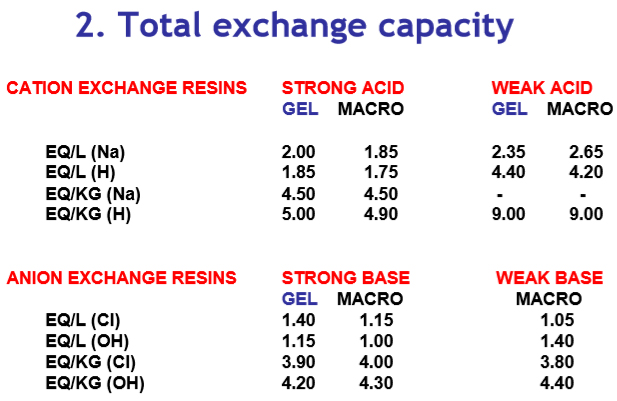
A capacidade de troca das resinas será diferente para cada tipo. Esta é uma medida do número total de sítios ativos que estão disponíveis para troca (eq/L ou eq/kg). Além disso, é induzida uma mudança no volume.
Os valores típicos para resinas em diferentes formas iónicas são:
Uma vez atingida a capacidade de troca, podemos dizer que a resina está esgotada. Quando isto acontece, a resina é regenerada. Este é um conjunto de operações que permite a deslocação dos iões retidos até que a resina volte ao seu estado inicial de carga.
A primeira operação do processo é a retrolavagem: a água é passada no sentido ascendente, provocando a descompactação do leito e a eliminação de possíveis partículas que possam ter sido retidas. Esta operação é realizada a uma velocidade crítica estabelecida pelo fabricante da resina.
Depois, na direção da lavagem, será introduzida uma solução regeneradora, que será de:
- HCL ou HSO4 para troca catiónica
- NaOH (soda cáustica) para troca de aniões
Esta operaçao e realizada com uma concentração controlada específica em cada caso. O leito é então lavado, que consiste em duas fases: uma lavagem lenta para assegurar que a solução regenerante chega a todo o leito, e uma lavagem rápida para remover qualquer solução regenerante restante e deixar a resina no estado ideal para iniciar um novo ciclo de trabalho.
O processo que ocorre durante a regeneração é o contrário do processo de esgotamento.
- Para resinas catiónicas: Na-R + HCl -> H-R + NaCl
- Para resinas aniónicas: Cl-R + NaOH -> R-OH + NaCl
As águas naturais contêm iões de cálcio e magnésio que formam sais pouco solúveis.
Estes catiões, entre outros catiões menos comuns como o estrôncio ou o bário, são chamados iões de dureza. Quando a água evapora, podem precipitar-se e formar sólidos.
A água dura produz incrustações e pode gerar turvação, pelo que é necessário eliminar estes componentes na medida do possível para conseguir uma água mais macia.
Para este fim, são utilizadas resinas de troca catiónica fortemente ácidas nas quais o ião permutável é Na de sódio, genericamente chamada resina catiónica no ciclo do sódio.
A reação de troca geral no processo de amolecimento que tem lugar pode ser expressa por:
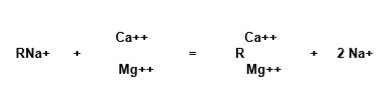
A resina de ciclo de sódio (RNa) entra em contacto com iões de cálcio e magnésio (Ca2+, Mg2+) e retém-nos, renunciando aos cátions de sódio para a água.
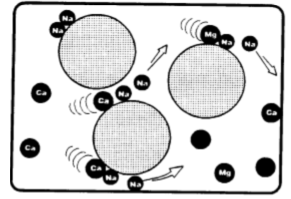
Os catiões de sódio cedidos pela resina ligam-se aos ânions aos quais o cálcio e o magnésio estavam ligados, formando o mesmo sal na forma de sódio. No caso dos bicarbonatos de cálcio e magnésio, temos:
Na suavização ou descalcificação, a salinidade da água tratada é a mesma que a da água a ser tratada, com a diferença de que os sais que continham os iões causadores da dureza são transformados em sais de sódio muito solúveis que não causam descamação.
Para o processo de regeneração da resina, será utilizada uma solução de salmoura (cloreto de sódio):
- Ca-R + 2NaCl -> CaCl2 + Na2 R